Ihre Aufgaben Sie akquirieren Neukunden und beraten unseren festen Kundenstamm mit Ihrem technischen Know-how und Ihrer Persönlichkeit. In Deutschland/Österreich betreuen Sie außerdem unseren Kundenstamm persönlich und bauen eine langfristige sowie vertrauensvolle Beziehung auf. Die Tätigkeit erfordert Reisebereitschaft und einen Führerschein (PKW). Für Dienstfahrten steht Ihnen ein Firmenwagen zur Verfügung. Sie beobachten den Wettbewerb und nehmen […]
Willkommen auf der Webseite der
S.P.L. Elektronik aus Brieselang
Ihr Ansprechpartner seit über 25 Jahren, wenn es um die Überprüfung von Sicherheits- und Funktionseigenschaften von elektrischen/medizinisch elektrischen Geräten/Systemen geht.
Neuigkeiten
Servicetechniker / Medizintechniker (m/w/d)
Ihre Aufgaben Sie führen Kalibrierungen, Prüfungen und Wartungen an unseren Mess- und Prüfgeräten durch. Sie führen Reparaturen an unseren Mess- und Prüfgeräten durch. Ihr Profil Sie haben eine abgeschlossene Ausbildung zum Medizintechniker, Elektroniker oder eine ähnliche Qualifikation. Sie haben ein technisches Grundverständnis. Sie handeln stets qualitäts- und kundenorientiert. Sollten Sie nicht alle obenstehenden Kriterien erfüllen, […]
GM-800 „NEU“!
GM-800 Die Entwicklung des Mess- und Prüfgeräts GM-800, zur Überprüfung der elektrischen Sicherheit, wurde über das Programm „Brandenburgischer Innovationsgutschein“ (BIG-FuE) bzw. durch Mittel von Bund/Land gefördert. Datenblatt
HF-Prüfung „LEICHT“ gemacht!
HF-400 HF-Chirurgie Tester zur Funktionsprüfung von HF-Chirurgiegeräten · Vorzugswiderstände einstellbar· normengerechte Prüfung· einfache Handhabung· ideal für unterwegs Datenblatt
AED-Prüfung „JETZT“ noch einfacher
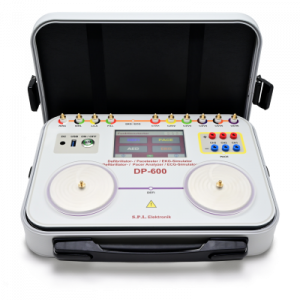
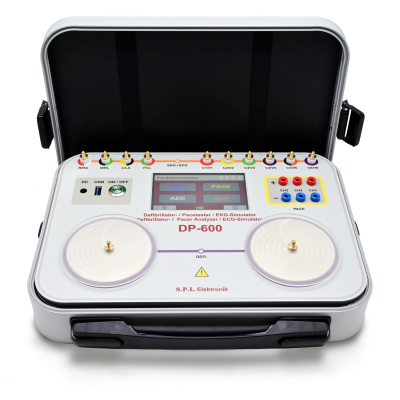
DP-600 Prüfgerät zur Funktionsprüfung von Defibrillatoren, externen Herzschrittmachern und EKG Simulation · Netz- oder Akkubetrieb · grafische Anzeige der Entladekurve · Touchscreen Bedienung oder PC-Steuerung · Stoppuhrfunktion für Lade- und Entladezeiten · polaritätsunabhängige Messung von Defi-Impulsen · Ein-, Zwei und Dreikreis-Herzschrittmacher Datenblatt